cho 6,486 gam hỗn hợp Ba và BaO vào nước dư thì thấy thoát ra 0,56 lít H2 (đktc)
a) viết các phản ứng sảy ra
b) tính phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu
Hòa tan 12,8 gam hỗn hợp A gồm (Fe và Fe2O3) vào dung dịch H2SO4 loãng 0,46M dư. Sau khi phản ứng kết thúc thu được 4,48 lít khi H2 (đktc).
a/ Viết các phương trình hóa học.
b/ Tính % theo khối lượng của mỗi chất có trong hỗn hợp A.
c/ Tính thể tích H2SO4 loãng tham gia phản ứng.
\(a,Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ b,n_{Fe}=n_{H_2}=0,2\left(mol\right)\\ \%m_{Fe}=\dfrac{0,2.56}{12,8}.100\%=87,5\%\\ \%m_{Fe_2O_3}=100\%-87,5\%=12,5\%\\ c,n_{Fe_2O_3}=\dfrac{12,8-11,2}{160}=0,01\left(mol\right)\\ n_{H_2SO_4}=n_{Fe}+3n_{Fe_2O_3}=0,2+3.0,01=0,23\left(mol\right)\\ V_{ddH_2SO_4}=\dfrac{0,23}{0,46}=0,5\left(M\right)\)
Cho 18.5 gam hỗn hợp X gồm Fe, Zn, Cu vào dung dịch H2SO4 loãng dư thu được 4,48 lit khí (dktc). Nếu cũng cho lượng hỗn hợp X trên vào H2SO4 đặc nóng, eư thì thu được 7,84 lit khí SO2 (dktc)
a) Tính thành phần trăm theo khối lượng của các kim loại trong hỗn hợp đầu
b) Dẫn lượng khí So2 thu được đi qua 200ml dd KOH 1M. Tính khối lượng và nồng độ mol các chất trong dd sau phản ứng
cho 5gam hỗn hợp bột bạc và đồng vào dung dịch AgNo3 dư , phản ứng hoàn toàn , thu 8,8 gam chất rắn . Tính thành phần trăm về khối lượng của đồng trong hỗn hợp ban đầu ?
Ag + AgNO3 (không phản ứng)
Cu + 2AgNO3 -> 2Ag +Cu(NO3)2
0.04 0.08
n(Ag)=8.8/108=0.08 mol
m(Cu)=0.04*64=2.56(g)
%m(Cu)=(2.56*100)/5=51.2%
cho 0,896 lít (đktc) hỗn hợp khí gồm CH4 và C2H4 tác dụng với oxi dư. lượng oxi tham gia phản ứng là 3,52 g
a, viết pt hoá học
b, tính phần trăm thể tích mỗi khí trong hỗn hợp
c, tính khối lương khí co2 tạo ra
CH4+2O2-to>CO2+2H2O
x---------2x-------x
C2H4+3O2-to>2CO2+2H2O
y-------------3y------2y
=>Ta có :
\(\left\{{}\begin{matrix}x+y=0,04\\2x+3y=0,11\end{matrix}\right.\)
=>x=0,01, y=0,03 mol
=>%VCH4=\(\dfrac{0,01.22,4}{0,896}100\)=25%
=>%VC2H4=75%
=>m CO2=(0,01+0,03.2).44=3,08g
a, ta có PTHH :
CH4 + 2O2 \(\Rightarrow\) CO2 + 2H2O (*)
C2H4 + 3O2 \(\Rightarrow\) 2CO2 + 2H2O(+)
b, Gọi x, y lần lượ là số mol của CH4 , C2H4 ( x, y > 0 )
Ta có : nh = \(\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
\(\Rightarrow x+y=0,04\left(mol\right)\) (1)
lại có no2 pứ = \(\dfrac{3,52}{32}=0,11\left(mol\right)\)
\(\Rightarrow2x+3y=0,11\left(mol\right)\) (2)
Từ (1) và (2) ta có hệ pt:\(\left\{{}\begin{matrix}x+y=0,04\\2x+3y=0,11\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,01\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
%VCH4 = \(\dfrac{0,01}{0,04}\times100\%=25\%\)
%VC2H4 = \(\dfrac{0,03}{0,04}\times100\%=75\%\)
c, Theo pt nCO2(*) = nCH4 = 0,01 (mol)
nCO2(+) = 2nC2H4 = 0,6 (mol)
\(\Rightarrow m_{co_2}=\left(0,01+0,6\right)\times44=26,84\left(g\right)\)
cho 1,36 g hỗn hợp khí CH4 ,C2H4 tác dụng vừa đủ với 3,584 lít oxi (đktc)
a, viết pthh
b, tính thành phần phần trăm theo khối lượng các khí có trong hỗn hợp
c, tính khối lượng nước hình thành sau phản ứng
CH4+2O2-to>CO2+2H2O
x---------2x-------x---------2x
C2H4+3O2-to>2CO2+2H2O
y-------------3y------2y-------2y
=>\(\left\{{}\begin{matrix}16x+28y=1,36\\2x+3y=0,16\end{matrix}\right.\)
=>x=0,05 mol , y=0,02 mol
=>%m CH4=\(\dfrac{0,05.16}{1,36}100\)=58,82%
=>%m C2H4=41,17%
=>mH2O=(0,1+0,04).18=2,52g
a, \(n_{O_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
PTHH: CH4 + 2O2 ---to→ CO2 + 2H2O
Mol: x 2x 2x
PTHH: C2H4 + 3O2 ---to→ 2CO2 + 2H2O
Mol: y 3y 2y
b,Ta có hệ pt: \(\left\{{}\begin{matrix}16x+28y=1,36\\2x+3y=0,16\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,05\left(mol\right)\\y=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{CH_4}=0,05.16=0,8\left(g\right)\Rightarrow\%m_{CH_4}=\dfrac{0,8.100\%}{1,36}=58,82\%\)
\(\Rightarrow\%m_{C_2H_4}=100\%-58,82\%=41,18\%\)
c, \(m_{H_2O}=\left(2.0,05+2.0,02\right).18=2,52\left(g\right)\)
Cho 6g hỗn hợp mg và cu vào dd axít clohiđric phản ứng sảy ra vừa đủ.Sau phản ứng người ta thu đc 4,48l khí (ở đktc).Tính khối lượng của mỗi kim loại trong hỗn hợp trên
Vì Cu không tác dụng với dung dịch axit clohidric loãng :
\(n_{H2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,2 0,2
\(n_{Mg}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{Mg}=0,2.24=4,8\left(g\right)\)
\(m_{Cu}=6-4,8=1,2\left(g\right)\)
Chúc bạn học tốt
Hòa tan 14,8 gam hỗn hợp gồm Fe và Cu vào lượng dư dung dịch hỗn hợp HNO3 và H2SO4 đặc nóng. Sau phản ứng thu được 10,08 lít NO2 (đktc) và 2,24 lít SO2 (đktc). Khối lượng Fe trong hỗn hợp ban đầu là:
A. 5,6
B. 8,4
C. 18
D. 18,2
Đáp án B
Gọi a, b lần lượt là số mol của Fe, Cu
56a + 64b = 14,8 (1)
Quá trình nhường electron:
Fe - 3e → Fe
a 3a
Cu - 2e → Cu
b 2b
→ ∑ne nhường = (3a + 2b) mol
Quá trình nhận electron:
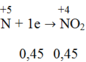
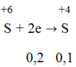
→ ∑ne nhận = 0,45 + 0,2 = 0,65 mol
Áp dụng định luật bảo toàn electron:
3a + 2b = 0,65 → a = 0,15 và b = 0,1 → mFe = 8,4 g
Cho 10g hỗn hợp Fe và Cu vào dd CuSO4 dư. Sau khi phản ứng xong thu được chất rắn có khối lượng là 11g , tính thành phần % theo khối lượng của Fe và Cu trong hỗn hợp đầu
Hỗn hợp A gồm các kim loại Mg, Al, Fe.
Lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch NaOH dư, sinh ra 3,36 lít khí (đktc). Mặt khác cũng lấy 14,7 gam hỗn hợp A cho tác dụng với dung dịch HCl dư, sinh ra 10,08 lít khí (đktc) và dung dịch B. Cho dung dịch B tác dụng với dung dịch NaOH dư, lọc kết tủa tạo thành và nung nóng trong không khí đến khối lượng không đổi thu được m gam chất rắn. Tính m và tính % theo khối lượng của mỗi kim loại trong hỗn hợp A.Cho hỗn hợp A tác dụng với dung dịch CuSO4 dư, sau khi phản ứng kết thúc, lọc lấy chất rắn đem hòa tan hết chất rắn trong dung dịch HNO3 loãng dư, thu được 26,88 lít khí NO (đktc). Tính khối lượng hỗn hợp A.1.1. Al + NaOH + H2O ==> NaAlO2 + 3/2H2
nH2(1)=3,36/22,4=0.15(mol)
=> nAl(1)= nH2(1):3/2= 0.15:3/2= 0.1(mol)
2.Mg + 2HCl ==> MgCl2 + H2
3.2Al + 6HCl ==> 2AlCl3 + 3H2
4.Fe + 2HCl ==> FeCl2 + H2
=> \(n_{H_2\left(2,3,4\right)}=\) 10.08/22.4= 0.45(mol)
=> nH2(3)=0.1*3/2=0.15(mol)
MgCl2 + 2NaOH ==> Mg(OH)2 + 2NaCl
AlCl3 + 3NaOH ==> Al(OH)3 + 3NaCl
FeCl2 + 2NaOH ==> Fe(OH)2 + 2NaCl